こんにちは、Xenoです!
今回は『SI(国際)単位系と状態量』について解説します。
私たちが普段よく使っている物理量はSI単位系と定められたものです。
そしてそれらは状態量かそうでないかに分けることができるのです。
この記事を読めば主に工業熱力学で使用するSI単位系と状態量と非状態量について把握することができます。
それでは行きましょう!
前回の記事はこちらからどうぞ!

SI(国際)単位系とは?
SI単位系とは、国際的に定められた世界共通の単位系です。
工業熱力学では主に以下のSI単位系が用いられます。

温度
熱力学では温度を摂氏温度(セルシウス温度)ではなく、絶対温度(ケルビン温度)で表します。
摂氏温度と絶対温度の関係は以下の通りです。
\[T=T_C+273.15[K]\]
摂氏温度や絶対温度に関しては以下の記事で詳しく解説しています!

圧力(絶対圧とゲージ圧)
圧力\(p\)は単位記号に\(Pa[N/m^2]\)を用いますが、主に『絶対圧』と『ゲージ圧』の2種類が存在します。
絶対圧
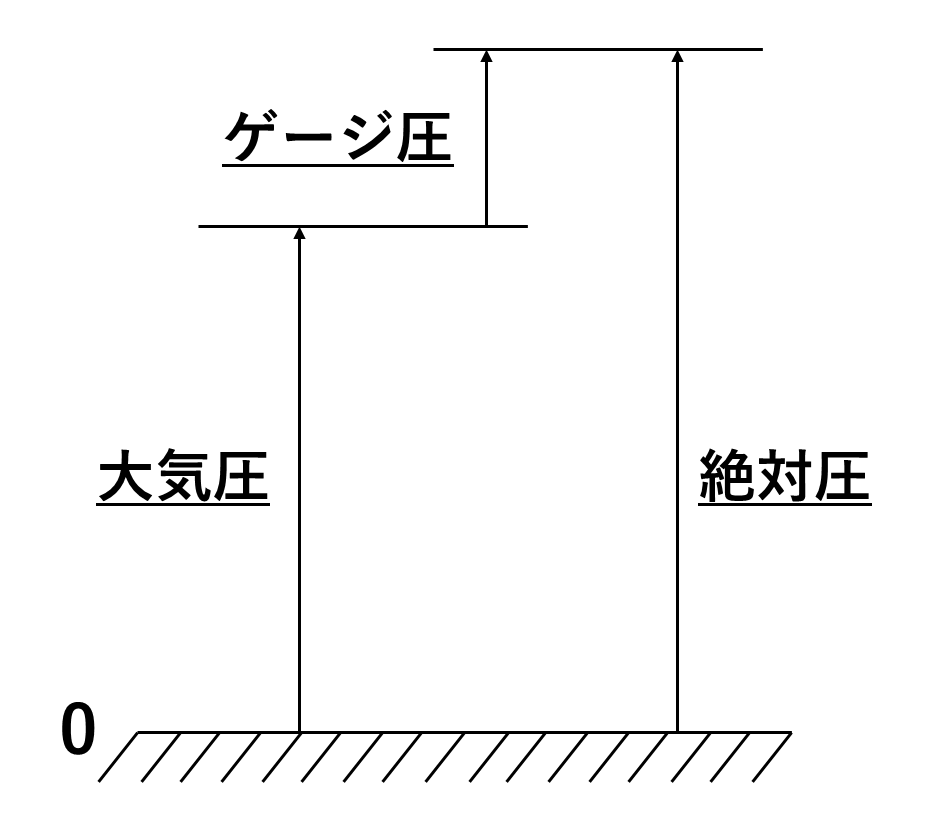
絶対圧は真空状態を基準とする圧力です。
工業熱力学ではこの圧力が用いられ、ゲージ圧と大気圧を調べることで簡単に求めることができます。
ゲージ圧
ゲージ圧は大気圧を基準とした圧力です。
ガスボンベなどに圧力計などを取り付けることによって、ゲージ圧を測定することが可能です。
大気圧
大気圧は気圧計などで測定できる大気による圧力です。
国際標準値に定められている標準大気圧は以下の通りです。
\[1[atm](標準大気圧)=101.3[kPa](=1013[hPa])\]
絶対圧とゲージ圧の関係は以下の式で表されます。
\[絶対圧=大気圧+ゲージ圧\]
仕事と動力(仕事率)
仕事
下図のように、物体を力\(F[N]\)で\(x[m]\)動かしたときの量を『仕事』といい、次の式で表されます。
\[L=Fx[J(Nm)]\]
今まで仕事は文字記号に『W』を用いるのが普通でしたが、工業熱力学においては『L』を用いるのが一般的です。しかし、教科書によっては『W』を用いることもあるので注意してください。
動力(仕事率)
単位時間あたりに行われる仕事は『動力(仕事率)』といいます。仕事率は以下のように定義されます。
\[1[W]=1[J/s]\]
\[1[PS(馬力)]=75×9.81[J/s]=735.5[W]\]
熱量と比熱
熱は系の境界を通じて移動するエネルギーの一種です。
熱量には主に2種類の表し方があります。
1[cal(カロリー)]
\(1[g]\)の水の温度を\(1[^\circ{C}]\)(正確には\(14.5[^\circ{C}]\)から\(15.5[^\circ{C}]\)まで)上昇させるのに必要な熱量
1[J(ジュール)]
\(1[N]\)の力のもとで\(1[m]\)動かすときの仕事
なぜ熱量に仕事と同じ[J(ジュール)]が用いられているかというと、1845年にジェームズ・プレスコット・ジュール(James Prescott Joule)がエネルギー保存則の研究(ジュールの実験)にて『仕事と熱はともに同じエネルギーである』ということを発見したからです。
なので、工業熱力学では熱量に[J(ジュール)]を用いるのが一般的です。
[cal]と[J]の関係は、次式で表されます。
\[1[kcal]=4.187[kJ]\]
また、質量1[kg]の物体の温度を1[℃]高めるのに必要な熱量は『比熱[kJ/kgK]』と呼ばれ、質量m[kg]の物体の温度を1[℃]高めるのに必要な熱量は『熱容量[kJ/K]』といいます。
比熱\(c\)と熱容量\(C\)の関係は次式で表されます。
\[C=cm[kJ/K]\]
1kgあたりの物理量
工業熱力学では、作動流体1[kg]あたりで物理量を考えることが多いです。
例えば、容積(体積)であれば1[kg]あたりの容積を『比容積\(v[m^3/kg]\)』と表します。
このように、文字記号は容積であれば大文字で\(V\)、比容積であれば小文字で\(v\)と表記します。
1[kg]あたりで考える物理量は主に以下のものがあります。
- 比容積\(v[m^3/kg]\)
- 比内部エネルギー\(u[J/kg]\)
- 比エンタルピー\(h[J/kg]\)
- 比エントロピー\(s[J/kgK]\)
状態量と非状態量
今までの物理量は『状態量』と『非状態量』に分けて考えることができます。
一つずつ見ていきましょう。
状態量
状態量とは、その時の状態だけで決まり、変化の経路には依存しない物理量です。
例えば温度が\(T_1\)から\(T_2\)に変化するとき、温度変化は次式のように表すことができます。
\[\int_1^2dT=T_2-T_1\]
上式を見ると温度変化は経路によらず、温度\(T_1,T_2\)のみで完結していることが分かります。
状態量である物理量は他に以下のものがあります。
- 温度\(T[K]\)
- 容積\(V[m^3]\)
- 圧力\(p[Pa]\)
- 内部エネルギー\(U[J]\)
- エンタルピー\(H[J]\)
- エントロピー\(S[J/K]\)
非状態量
非状態量とは、その時の状態だけで決まらず、変化の経路によって異なる値を持つ物理量です。
主な非状態量の物理量は以下のものが挙げられます。
- 仕事\(L[J]\)
- 熱量\(Q[J]\)
しかし、これらは状態量のようには表せないので、工業熱力学では次のように表すことが多いです。
\[\int_1^2dL=L_{12}\]
\[\int_1^2dQ=Q_{12}\]
状態量のように2つの状態の差では表せないので注意してください。
まとめ
今回は『SI(国際)単位系と状態量』について解説しました。
使用する物理量が状態量なのか、それとも状態量ではないのかを考えることは工業熱力学では非常に重要です。
今回取り上げたものだけでもしっかりと覚えておきましょう。
次回は『絶対仕事(膨張仕事)と工業仕事(機関仕事)』について解説します。
それでは、また次の記事でお会いしましょう!








コメント